Електролізом називають явище виділення речовини на електродах, що відбувається, коли крізь електроліт проходить постійний електричний струм. При цьому на катоді відбувається реакція відновлення катіонів. Вона пов'язана з приєднанням електронів до катіонів. На аноді відбуваються реакції оксидування, пов'язані з віддачею електронів аніонами.
Явище електролізу кількісно вивчав М. Фарадей. Він вперше зробив поділ продуктів електролізу на первинні та вторинні. У 1833 р. М. Фарадей за допомогою дослідів встановив два закони електролізу, які названо його ім'ям.
Перший закон Фарадея формулюється так: маса т речовини, що виділяється на кожному з електродів, прямо пропорційна зарядові q, який пройшов крізь електроліт, тобто
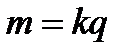 , (10.4)
, (10.4)
де k — електрохімічний еквівалент, неоднаковий для різних речовин. Він чисельно дорівнює масі речовини, яка виділяється під час електролізу при проходженні крізь електроліт заряду q = 1 Кл. Якщо крізь електроліт проходить постійний електричний струм I протягом часу t, то q=It і рівняння (10.4) записують у вигляді
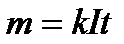 . (10.5)
. (10.5)
Якщо сила струму змінюється з часом, то
 .
.
Другий закон Фарадея вказує на те, що електрохімічні еквіваленти речовин прямо пропорційні їх хімічним еквівалентам:
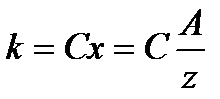 , (10.6)
, (10.6)
де С — коефіцієнт пропорційності, який має однакове значення для всіх речовин. Хімічним еквівалентом х називають відношення атомної маси А до валентності z речовини. Замість сталої С користуються оберненою до неї величиною, яку називають числом Фарадея і позначають F = 1/С. Тоді рівняння (10.6) перепишеться так:
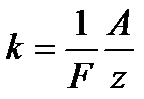 . (10.7)
. (10.7)
На основі формул (10.4) і (10.7) одержують об'єднаний закон Фарадея
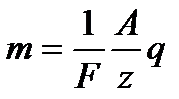 , (10.8)
, (10.8)
або
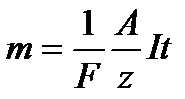 . (10.9)
. (10.9)

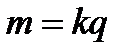 , (10.4)
, (10.4)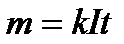 . (10.5)
. (10.5) .
.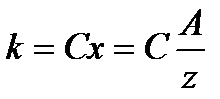 , (10.6)
, (10.6)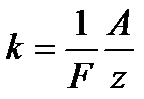 . (10.7)
. (10.7)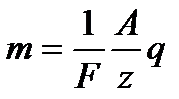 , (10.8)
, (10.8)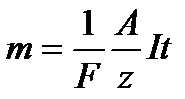 . (10.9)
. (10.9)