1.4.1. Внутрішня енергія
Термодинамічні потенціали – визначені функції об’єму, тиску і температури, ентропії та інших макропараметрів, що характеризують стан термодинамічної системи. В кожній комбінації незалежному параметру відповідає свій термодинамічний потенціал. Зміни потенціалу, що відбуваються в ході процесів, визначають роботу, що здійснює тіло, або отриману системою теплоту, або вказує напрям даного процесу. При розгляданні термодинамічного потенціалу, використовують рівняння першого закону термодинаміки у вигляді рівняння:
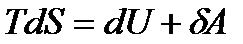 .
.
Так як термодинамічний потенціал є функцією стану системи, то приріст будь-якого потенціалу дорівнює повному диференціалу функції. Повний диференціал функції f(x;y) змінних x і y визначається виразом:
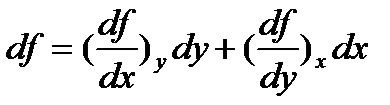 . (1)
. (1)
Тому якщо в ході перетворень для приросту величини f отримуємо вираз, що має вигляд:
df=x(A;B)dA +y(A;B)dB , (2)
то можна стверджувати, що величина f - функція змінних А і В, причому функції x(A;B), y(A;B) – частинні похідні функції f(A;B). Тоді:
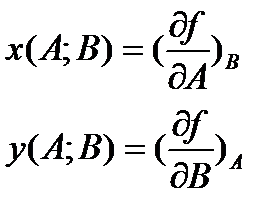 . (3)
. (3)
З першого закону термодинаміки для обернених процесів, зміна внутрішньої енергії dU=TdS-pdV згідно з рівнянням (2) і (3), знаходимо:
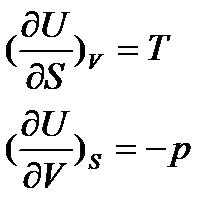 . (4)
. (4)
Співставляючи (4) і (2), бачимо, що в якості так-званих природних змінних внутрішньої енергії виступають змінні ентропії і об’єму. При відсутності теплообміну з зовнішнім середовищем:
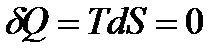 ,
,
і робота дорівнює зменшенню внутрішньої енергії тіла:
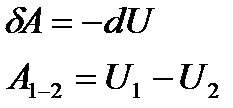 . (5)
. (5)
Формула (5) справедлива як при обернених, так і при необернених процесах. При V=const 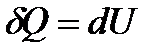 .
.
Об’ємна теплоємність:
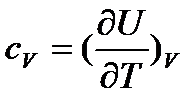 . (6)
. (6)

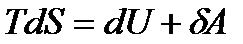 .
.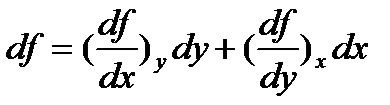 . (1)
. (1)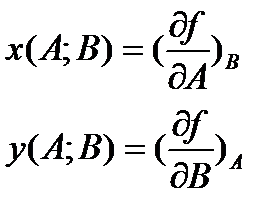 . (3)
. (3)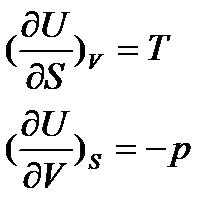 . (4)
. (4)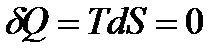 ,
,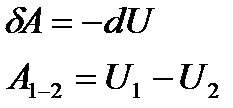 . (5)
. (5)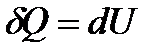 .
.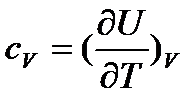 . (6)
. (6)