1.2.1. Внутрішня енергія термодинамічної системи
Будь-яка термодинамічна система в будь-якому стані володіє повною механічною енергією, що включає:
1. кінетичну енергію механічного руху усієї системи як цілу, так і її макроскопічних частин;
2. потенціальну енергію, яка залежить від положення системи в зовнішньому силовому полі (гравітаційному, електричному, магнітному);
3. внутрішню енергію U, яка залежить лише від внутрішнього стану системи.
В термодинаміці розглядають макроскопічні умовно-нерухомі системи без урахування їх потенціальної енергії в зовнішніх силових полях.
Значення повної і внутрішньої енергії співпадає, тому поняття внутрішньої енергії – одне з основних понять в термодинаміці.
До складу внутрішньої енергії входить енергія різних видів руху і взаємодій одна з одною усіх частинок (атомів, молекул, іонів, електронів та ін.),що утворюють систему, яка розглядається. Наприклад до внутрішньої енергії газоподібного тіла входять:
1. кінетична енергія хаотичного (теплового, поступального і обертального руху молекул);
2. кінетична і потенціальна енергія коливань атомів в молекулі;
3. потенціальна енергія, що обумовлена силами міжмолекулярних взаємодій;
4. енергія взаємодії електронів в атомах і молекулах між собою і в ядрах;
5. тенергія руху і взаємодії нуклонів в ядрі або в ядрах.
Зміна внутрішньої енергії при переході з деякого стану 1 в 2 не залежить від виду процесу переходу, а залежить від початку і кінця стану цієї системи. Наприклад, якщо в результаті якого-небудь процесу система повертається в початковий стан, то повна зміна її внутрішньої енергії чисельно:
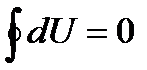 . (1)
. (1)
Приріст внутрішньої енергії dU є повним диференціалом термодинамічної координати, а внутрішня енергія є однозначною функцією термодинамічної системи. Внутрішня енергія термодинамічної системи залежить тільки від температури і зовнішніх параметрів системи. Наприклад, внутрішня енергія U деякої системи постійної маси m залежить від температури T і об’єму системи V системи:
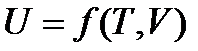 . (2)
. (2)
Внутрішня енергія подібно до потенціальної енергії в механіці може бути визначена з точністю до деякої сталої , яка залежить від вибору стану, в якому внутрішня енергія системи приймається рівною нулю.
В термодинаміці визначається не абсолютне значення внутрішньої енергії, а лише її зміна в процесах, які розглядаються, тому в термодинаміці під внутрішньою енергією розглядаються тільки ті її складові, які змінюються в тих термодинамічних процесах, які розглядаються. З урахуванням цього під внутрішньою енергією реального газу можна розуміти складові 1, 2, 3, а під внутрішньою енергією U ідеального газу – складову 1 повної внутрішньої енергії газоподібного тіла.

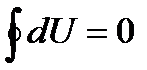 . (1)
. (1)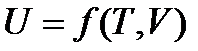 . (2)
. (2)